米疾病管理予防センター(CDC)は7月21日、新型コロナウイルス(中共ウイルス)について、緊急使用許可(EUA)を得ていたコロナ単独を検査するPCR検査体制「CDC 2019-Novel Coronavirus (2019-nCoV) Real-Time RT-PCR Diagnostic Panel」を年内までに廃止すると発表した。今後は、コロナほかインフルエンザも同時に検査できる効率的な手法を取るよう医療機関に促している。
廃止の理由について、CDCは次のように説明している。米国はウイルス流行初期の2020年2月、コロナウイルス検査体制の設置のために、米国食品医薬品局(FDA)に対して、PCR検査の緊急使用許可を申請した。当時はこの方法以外効果的な検査がなかった。
しかし、現在はすでに民間企業などが開発した数百種類の検査手法がFDAにより承認されている。これらは、PCR検査体制よりも効率の良い処理能力を備え、一度に複数の病気を確認できるものが多いという。
CDCは、公衆衛生検査機関に向けて、今後の流行が見込まれる季節性インフルエンザなどと同時に検査ができる多重検査の準備を促している。推奨する多重検査について、SARS-CoV-2(新型コロナウイルス)、インフルエンザウイルスA型、B型のRNAを検出し、識別できると説明している。
CDCは公衆衛生のために、限られた医療資源を確保するため、よりニーズの低くなったPCR検査体制を段階的に縮小させ、年内には廃止する。
PCR検査をめぐって、その正確性を疑問視する声があがっていた。ウイルスの検出に必要なサイクル数(Ct値)に国際的な標準はなく、値が高ければウイルスが少なくても陽性と診断されるからだ。また、死んだウイルスの断片と生きた感染性ウイルスを区別できない場合もあり、偽陽性のリスクが高まるという懸念もあった。
CDCは昨年11月、PCR検査の基準値について、「患者のウイルス量や感染力、隔離期間を判断するために使用すべきではない」と説明している。
世界保健機関(WHO)も今年1月20日に、新型コロナウイルスの診断についてはPCR検査と並行して患者の既往歴や疫学的な危険因子も考慮すべきであると伝え、「ほとんどのPCR検査は診断の補助である」とするガイドラインを発表している。
(翻訳編集・郭丹丹)
※誤読を招く可能性がある表現があり、9月2日、加筆・訂正いたしました。(大紀元日本語編集部)



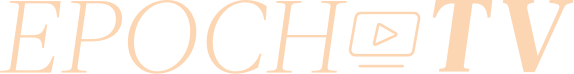










 ご友人は無料で閲覧できます
ご友人は無料で閲覧できます Line
Line Telegram
Telegram











ご利用上の不明点は ヘルプセンター にお問い合わせください。