ファイザー社の開発中のインフルエンザワクチンは、高齢者をインフルエンザから守ることを証明する新たなデータがない限り、承認されないだろうと、食品医薬品局(FDA)長官が新たなインタビューで示唆した。
このメッセンジャーリボ核酸(mRNA)注射は「高齢者に対する有効性を示せなかった」と、FDA長官のマーティン・マカリー博士が11月29日のフォックス・ニュース出演時に述べた。
「試験はゼロベネフィットを示した」と同氏は述べている。
「我々は、臨床試験で不成功に終わった、効かない新製品にただお墨付きを与えるつもりはない。データがないまま物事にお墨付きを与えるなら、科学を愚弄することになる」
ファイザー社のメディアチームはエポックタイムズのコメントの求めに応じなかった。
ファイザー社などの研究者は、最近『ニューイングランド・ジャーナル・オブ・メディスン(NEJM:英文臨床系医学雑誌のなかで最も権威あるとされる雑誌)』に掲載された論文で、この実験的mRNAワクチンは、健康な18歳から64歳の人々を対象とした試験で、既に承認されている他社のワクチンよりも優れた成績を収めたと述べた。
研究者らは、同じ試験でワクチン接種を受けた高齢者の間で、0.5%がインフルエンザの症状を呈し、実際に感染が確認されたというデータについては、論文に記載しなかった。この割合は、認可済みワクチン接種者と全く同じであり、新ワクチンの優位性が示せなかった。
さらに、ファイザー社のワクチン接種後7日以内に有害反応を報告した高齢者は、既存ワクチンの接種者25.8%に対し、68.7%と遥かに多かったことも結果は示している。
この試験における高齢者の結果は、今年の初めにClinicalTrials.govに投稿され、論文の公開後、独立系ジャーナリストや、マサチューセッツ工科大学のレツェフ・レヴィ教授を含む、ワクチンに関する疾病対策センター(CDC)の諮問委員会メンバーによって強調された。
「私はこれを査読プロセスにおける重大な誠実性の欠如と見なす。NEJM編集委員会は、この失敗がどのように発生したのか明確な説明を提供し、著者に対し、現在の論文を訂正し、試験の全結果を報告するよう要求すべきである」とレヴィ氏はEメールでエポックタイムズに語った。
高齢者の結果が論文に含まれなかった理由を尋ねたところ、同誌の広報担当者はエポックタイムズに対し、Eメールで「研究著者が質問に最もよく答えられる」と述べた。
ファイザー社に勤務する筆頭著者からの問い合わせへの返答はなかった。
マカリー氏の発言は、FDAの生物学的製剤評価研究センターを率いるヴィナイ・プラサド博士が、当局が現在のインフルエンザワクチン枠組みを改訂する予定であるとの覚書を記した後に行われた。同氏はこれを「低品質な証拠データ、信頼性の乏しい検査法、不適切な症例対照研究に基づく効果測定」による「惨状」として全面的に見直す方針を示した。
現在の枠組みでは、流行が予測される株を標的とした更新版のワクチンが毎年承認されている。
FDAは、2024年に更新されたウェブサイトのページで、FDA承認のインフルエンザワクチンは「安全で効果的である」と述べている。CDC当局者は、2009年以降のインフルエンザに対するワクチンの有効性は19%から60%の範囲であると推定している。
プラサド氏はまた、ほとんどの新しいワクチンに関して、当局は病気の予防といった最終的な効果(臨床エンドポイント)に基づいて有効性を証明する、厳格なランダム化臨床試験を義務づけることになると述べた。
CDC諮問委員会のインフルエンザ作業部会を率いるロバート・マローン博士は、この覚書は「インフルエンザワクチン接種、年次ワクチン接種事業全体が今、大きな混乱にさらされている」ことを意味するとエポックタイムズに語った。




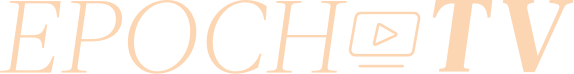








 ご友人は無料で閲覧できます
ご友人は無料で閲覧できます Line
Line Telegram
Telegram











ご利用上の不明点は ヘルプセンター にお問い合わせください。